戰船醫療
階段
E係列 |活著總了
52.52美元最後提出了
18美元 | 10年前缺失:戰船醫療的產品演示和案例研究
促進你的產品提供技術買家。
達到1000年代的買家使用CB的見解來確定供應商,演示產品,188bet游戏做出購買決定。
缺失:戰船醫療的產品&微分器
不要讓你的產品被跳過。買家使用我們的供應商排名名單公司和驅動(rfp)請求建議。
集合包含戰船醫療專家
專家集合是analyst-curated列表,突出了公司你需要知道的最重要的技術空間。
戰船醫療中1專家收集,包括醫療設備。
醫療設備
3088件
公司已獲得至少510 (k)自2014年以來,由美國食品和藥物管理局。公司標記# FDA510 (K)
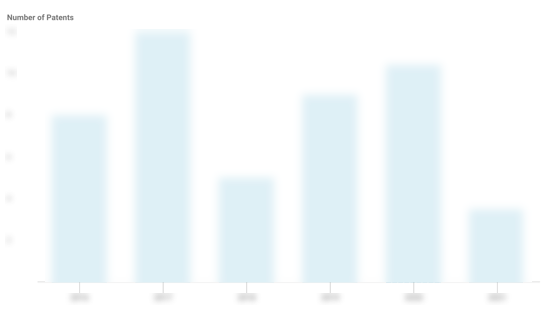
戰船醫療專利
戰船醫療提起了25項專利。
3最受歡迎的專利主題包括:
- 心髒手術
- 血管疾病
- 介入性心髒病學
申請日 |
授予日期 |
標題 |
相關的話題 |
狀態 |
|---|---|---|---|---|
|
10/29/2019 |
2/21/2023 |
血管疾病、血液學、血管手術,介入放射學,血管學 |
格蘭特 |
申請日 |
10/29/2019 |
|---|---|
授予日期 |
2/21/2023 |
標題 |
|
相關的話題 |
血管疾病、血液學、血管手術,介入放射學,血管學 |
狀態 |
格蘭特 |
最新的戰船醫療新聞
2023年2月13日
分享這篇文章分享這篇文章提供的新聞華盛頓2月13日2023 / MCRA從LLC領先的醫療設備集中管理谘詢公司和臨床研究機構(CRO)整合美國和國際監管事務,臨床試驗操作,還款和市場準入,醫療合規、網絡安全、質量保證,和日本銷售物流(DMAH)高興地宣布其作用成功上市前的批準(PMA)應用程序決定由美國食品和藥物管理局(FDA)批準巧克力觸摸®藥物塗層球囊(DCB)經皮導管腔間血管成形術。這種創新的紫杉醇塗層PTA氣球導管,由戰船醫療、LLC對待患者外周動脈疾病(PAD)的表麵股膕動脈。MCRA監管事務的專家和質量保證團隊與戰船醫學密切合作,實現這一重要的裏程碑。MCRA為首的副總裁和心血管監管事務和前FDA分支介入性心髒病學主任設備,邁克爾•約翰MCRA監管事務的高級主任,前副主任外部節奏和速度設備介入心髒病學的主要評論家設備尼基巴蒂斯塔,MCRA的高級主管丹•戈爾茨坦質量保證MCRA團隊合作與戰船在科學的各個方麵,監管和生產組件的PMA協助戰船醫療實現PMA批準藥物塗層球囊巧克力聯係。MCRA邁克爾•約翰的副總裁和心血管監管事務負責人表示“批準DCB巧克力觸摸標誌著一個新標準的性能,我們榮幸扮演了一個角色在這個重要PMA戰船醫療批準。”Glenn Stiegman, Senior Vice President of Clinical and Regulatory Affairs at MCRA, said "MCRA set out in 2019 to build the industry leading cardiovascular medical device consulting firm. Today, this is evidenced by the successful outcome the MCRA team has helped TriReme Medical achieve. We thank TriReme Medical for allowing us to be involved in this important PMA approval to help improve cardiovascular health for patients suffering with peripheral artery disease in the United States." Shiva Ardakani, SR. VP of RA/QA & Compliance at TriReme Medical, LLC said "The Chocolate Touch is a novel platform to treat PAD while minimizing the need for stents and represents a significant advancement in the therapeutic options for patients suffering with PAD. We are pleased to have partnered with such a skilled regulatory and quality consulting firm to bring this innovative cardiovascular product to patients in need." About MCRA, LLC: MCRA is the leading privately held independent medical device, diagnostics and biologics Clinical Research Organization (CRO) and advisory firm. MCRA delivers to its client's industry experience, integrating its six business value creators: regulatory, clinical research, reimbursement, healthcare compliance, quality assurance, and distribution logistics to provide a dynamic, market-leading effort from innovation conception to commercialization. MCRA's integrated application of these key value-creating initiatives provides unparalleled value for its clients. MCRA has offices in Washington, DC, Hartford, CT, New York, NY, and Tokyo, Japan and serves nearly 1,000 clients globally. Its core focus areas of therapeutic experience include orthopedics, spine, biologics, cardiovascular, diagnostic imaging, wound care, artificial intelligence, dental, anesthesia, general surgery, digital health, neurology, robotics, oncology, general and plastic surgery, urology, and in vitro diagnostic (IVD) devices and medical device cybersecurity. www.mcra.com About Viscogliosi Brothers, LLC: Viscogliosi Brothers, LLC (VB), founded MCRA in 2004. VB is headquartered in New York City and specialized in funding venture capital, private equity, and merchant banking activities for the neuromusculoskeletal industry. VB is dedicated to financing healthcare innovation. www.vbllc.com About TriReme Medical LLC: TriReme Medical, LLC, a subsidiary of QT Vascular, is a US medical device company based in Pleasanton, California. Founded in 2005, it is dedicated to developing, manufacturing and distributing advanced therapeutic solutions for the treatment of complex vascular disease. Addressing specific unmet clinical needs, TriReme is working with leading engineers and global thought leaders to offer physicians new and differentiated devices to improve outcomes in complex peripheral and coronary interventions. www.qtvascular.com/us/ For more information, please contact: Alyssa Howard, Vice President, Business Development SOURCE MCRA, LLC
戰船醫療常見問題(FAQ)
戰船醫療的總部在哪裏?
戰船醫療的總部位於7060 Pkwy谘詢中心,而往常。
戰船醫學的最新一輪融資是什麼?
戰船醫學的最新一輪融資係列E。
戰船醫療籌集了多少錢?
戰船醫療籌集了總計52.52美元。
戰船醫療的投資者是誰?
投資者戰船醫學包括三拱夥伴,亞當斯街夥伴,EDBI和設計資本。
戰船醫療的競爭對手是誰?
競爭對手戰船醫學包括Tryton醫療、ArraVasc莧菜醫療、IDev技術、靈活的支架解決方案和12。
比較戰船醫療競爭對手

Endologix開發商和製造商的微創治療血管疾病。Endologix關注其專利技術的開發和營銷治療腹主動脈瘤(AAA)。動脈瘤是主動脈的血管壁的削弱,人體最大的動脈。動脈瘤疾病引起的死亡在美國,據估計,170萬人55歲以上有AAA。每年,醫生診斷與AAA大約有200000人在美國。Endologix目前營銷Powerlink交付係統,整體內腔支架用於治療AAA (ELG)與銷售支架方案相比具有顯著的優勢。Powerlink自1999年以來一直在歐洲商用。FDA批準Powerlink AAA支架收到10月29日,2004年。Powerlink優越設計是由17個美國專利361允許索賠;這項技術是第一代ELGs旨在克服不足之處。設備銷售在美國和選定的國際市場。Endologix是對上市公司在納斯達克交易:ELGX。 The company's corporate office is located in Irvine, California.
苗條的醫療係統從事高度交付氣球充氣支架的發展。苗條的id是為了實現臨床,時間和成本節約的好處直接支架在一個單一的平台。苗條的正在開發的西羅莫司洗脫支架非炎症性質,可能減少刺激性的船比支架與典型的聚合物塗層襯裏。苗條的DES正在開發的有相同的藥物釋放動力學的市場領導者,可能減少炎症血管減少長期雙重抗血小板治療的必要性。

Tryton醫療是一個支架係統開發商治療分叉病變。Tryton端分支支架係統建立分支使用Tri-ZONE技術提供一個專門的策略治療分叉病變。Tryton鈷鉻支架是部署在使用標準的單線balloon-expandable側枝動脈支架輸送係統。然後將傳統藥物洗脫支架放置在主容器。支架係統獲得了CE標記和商用整個歐洲,俄羅斯和中東。它在美國被批準用於臨床實驗的使用。
膠束技術旨在彙集的臨床優勢藥物洗脫支架與裸金屬支架的長期安全穩定。
SquareOne正在開發一個支架輸送係統。
支架係統發展血管成形術導管和導絲和相關介入產品
發現正確的解決方案為您的團隊
CB見解188bet游戏科技市場情報平台分析數百萬數據點在供應商、產品、合作關係,專利來幫助您的團隊發現他們的下一個技術解決方案。